Lo que Necesita Saber
La posibilidad de usar células madre para curar la ceguera inspira titulares y llena los corazones de esperanza. Para quienes conviven con la pérdida de visión debido a enfermedades degenerativas de la retina, es crucial entender qué es un hecho y qué sigue siendo una promesa.
Este artículo ofrece una visión sobria y detallada de los avances, centrándose en la terapia celular OpCT-001 de BlueRock Therapeutics.
La idea central es revolucionaria: cultivar en laboratorio células fotorreceptoras (las células que captan la luz) a partir de células madre pluripotentes inducidas (iPSCs). Estas nuevas células se inyectan luego bajo la retina del paciente para reemplazar a las que fueron destruidas por la enfermedad. El objetivo final es restaurar la capacidad del ojo para “ver”.
El primer ensayo clínico en humanos (Fase 1/2a), registrado bajo el identificador NCT05908276, ha sido autorizado e iniciado 1. El enfoque principal de esta fase inicial no es demostrar la cura, sino evaluar la seguridad del procedimiento y la tolerabilidad del trasplante.
A pesar del enorme potencial, la terapia enfrenta desafíos significativos. El principal es la necesidad de medicamentos inmunosupresores para evitar que el cuerpo del paciente rechace las nuevas células. Además, la tecnología aún no ha sido aprobada para uso comercial y su costo inicial, cuando esté disponible, será probablemente muy elevado.
Los desafíos clave de la terapia: la barrera inmunológica y el alto costo financiero. (Crédito de la imagen: engeAI.com)
🧬 1. La Ciencia: Reconstruyendo la Retina
El OpCT-001 tiene como objetivo tratar enfermedades como la retinosis pigmentaria, donde mutaciones genéticas causan la muerte progresiva de los fotorreceptores (conos y bastones). Sin ellos, la retina pierde su capacidad de convertir la luz en señales neuronales, lo que conduce a la ceguera.
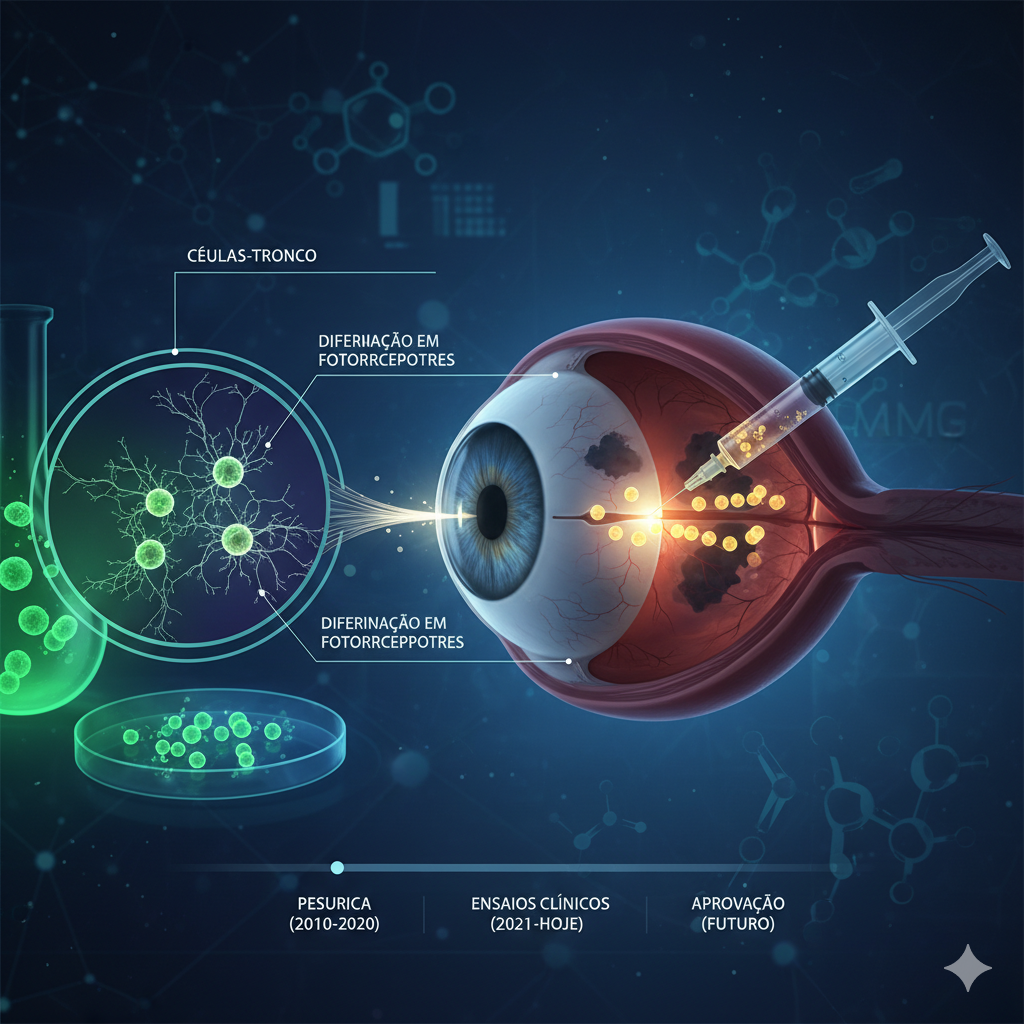
La terapia de BlueRock actúa en tres pasos principales:
- Creación: Células adultas se reprograman en laboratorio para convertirse en iPSCs.
- Diferenciación: Las iPSCs se cultivan cuidadosamente para convertirse en células precursoras de fotorreceptores.
- Trasplante: La suspensión con millones de estas nuevas células se inyecta en el espacio subretiniano para que puedan integrarse con el tejido existente 2.
La concesión de la designación “Fast Track” por parte de la FDA en febrero de 2024 reconoce la gravedad de la afección y el potencial de la terapia, pero es un facilitador burocrático, no un sello de aprobación 3.
🔬 2. Estado del Ensayo Clínico y Qué Esperar
El estudio clínico de Fase 1/2a es el primer paso en un largo viaje 1. Sus objetivos son pragmáticos y metódicos.
| Fase del Estudio | Objetivo Primario | Qué se Observa |
|---|---|---|
| Fase 1/2a (Actual) | Seguridad y Tolerabilidad | Evaluar si el procedimiento causa inflamación, rechazo, desprendimiento de retina u otros efectos adversos graves. |
| Fase 2 (Futuro) | Eficacia Preliminar y Dosis | Verificar si hay signos de mejora en la función visual y determinar la dosis óptima de células. |
| Fase 3 (Futuro) | Confirmación de la Eficacia | Comparar la terapia con un grupo de control en un gran número de pacientes para probar el beneficio clínico. |
Hasta la fecha, no se han publicado datos de eficacia para el OpCT-001 en humanos. Cualquier noticia sobre “cura” es prematura y especulativa.
⚠️ 3. Los Obstáculos Reales en el Camino
La promesa de la terapia celular es inmensa, pero los desafíos son igualmente grandes.
Inmunosupresión Continua: Por usar células de un donante estándar (alogénicas), la terapia requiere que el paciente tome medicamentos antirrechazo. Aunque el ojo goza de cierto “privilegio inmunitario”, este no es absoluto 4. Estos fármacos comprometen el sistema inmunitario y tienen sus propios efectos secundarios.
Integración Celular: No basta con inyectar las células; deben sobrevivir, organizarse en la compleja arquitectura de la retina y formar conexiones funcionales con las neuronas existentes, un desafío monumental 2.
Realidad de la Industria: El desarrollo de una terapia como esta cuesta cientos de millones de dólares. Esta presión financiera se refleja en las decisiones corporativas. Entre 2023 y 2024, BlueRock realizó despidos y cerró su centro de I+D en Cambridge, Massachusetts, para “priorizar el pipeline”, revelando la dura realidad de la industria 5.

El proceso de la terapia OpCT-001: desde el cultivo de células madre hasta su diferenciación en fotorreceptores y el trasplante subretiniano. (Crédito de la imagen: engeAI.com)
🔮 4. El Futuro: Esperanza Sobria
El OpCT-001 representa un avance genuino. La posibilidad de reemplazar células perdidas en la retina es, por primera vez, una realidad clínica en fase de prueba.
Sin embargo, el camino hacia una cura funcional, segura y accesible es largo. El objetivo final del campo es desarrollar terapias que no requieran inmunosupresión, quizás a través de la edición genética 6. Para los pacientes y sus familias, el mensaje es de una esperanza cautelosa. La ciencia avanza, pero lo hace a su propio ritmo: metódico y riguroso. La comprensión honesta del proceso es lo que verdaderamente nos permite acompañar y apoyar el avance de la ciencia.
Referencias
ClinicalTrials.gov. “A Study of OpCT-001 in Adult Participants With Primary Photoreceptor Diseases (STARGAZE).” Identificador NCT05908276. ↩︎ ↩︎
Mandai, M., et al. “Autologous Induced Pluripotent Stem-Cell–Derived Retinal Cells for Macular Degeneration.” New England Journal of Medicine, 2017. ↩︎ ↩︎
BlueRock Therapeutics. Anuncios relacionados con la designación “Fast Track” por la FDA, Febrero de 2024. ↩︎
Forrester, J.V., et al. “The eye’s immune privilege.” Trends in Immunology, 2008. ↩︎
FierceBiotech. Noticias sobre la reestructuración de BlueRock Therapeutics, 2023-2024. ↩︎
Cyranoski, D. “The CRISPR-edited immune-evading stem cells aiming for universal therapies.” Nature Biotechnology, 2024. ↩︎