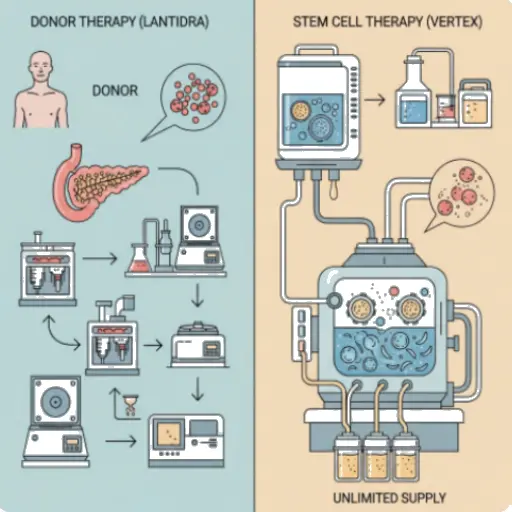
1. El Hito Histórico que Nadie Escalaría
En junio de 2023, la FDA dio luz verde a Lantidra, la primera terapia celular para la Diabetes Tipo 1 (DM1). El logro fue innegable: un procedimiento que trasplanta islotes pancreáticos de donantes fallecidos a pacientes con la forma más grave de la enfermedad demostró ser capaz de restaurar la producción de insulina y eliminar la necesidad de inyecciones diarias 1. Para la comunidad de pacientes, fue un rayo de luz. Para los analistas de la industria e inversores, sin embargo, la aprobación confirmó una sospecha de largo tiempo: el enfoque, aunque científicamente válido, es un callejón sin salida en términos de escala y acceso.
Lantidra es una terapia artesanal y de excepción. Sus tres barreras fundamentales no son pequeñas optimizaciones, sino características intrínsecas de su diseño:
- La Barrera Inmunológica: Requiere un régimen pesado y continuo de inmunosupresión, con todos los riesgos asociados.
- La Barrera Logística: La escasez de donantes de páncreas es su talón de Aquiles. Fuentes del área de trasplantes confirman que, debido al bajo rendimiento del proceso de aislamiento, se necesitan los páncreas de dos a tres donantes para tratar a un solo paciente. Esto limita la terapia a, como máximo, unos pocos cientos de personas por año, en un universo de millones.
- La Barrera Económica: Con costos que pueden superar los $200,000 USD por procedimiento, Lantidra se destina solo a casos de salud críticos, donde el riesgo de la hipoglucemia severa supera los riesgos y costos del tratamiento 2. Es una solución de nicho, no de salud pública.
2. La Validación Inadvertida: Cómo Lantidra Probó la Tesis de Vertex
Paradójicamente, el éxito limitado de Lantidra fue la mejor validación externa que la estrategia de Vertex Pharmaceuticals podría haber recibido. La aprobación de Lantidra respondió a la pregunta más fundamental de todas para reguladores e inversores: "¿funciona la terapia de reemplazo celular para la DM1?". La respuesta fue un rotundo “sí”.
Lantidra probó la biología. Con eso, eliminó el mayor riesgo científico del camino, dejando a Vertex libre para centrarse en el problema que nació para resolver: el de la ingeniería.
La tesis de inversión en Vertex, que justificó la adquisición de Semma Therapeutics por casi mil millones de dólares, nunca fue sobre el descubrimiento inicial, sino sobre la capacidad de transformar una ciencia de laboratorio en una solución industrial. La estrategia de la empresa se basa en dos pilares de ingeniería:
Pilar 1: Resolver la Escala (El Éxito del VX-880)
El ensayo clínico del VX-880 probó el primer pilar. Usando células madre, Vertex creó una fuente ilimitada y estandarizada de células beta, eliminando por completo la barrera logística de los donantes. Datos de congresos como el de la Asociación Americana de Diabetes (ADA) muestran un éxito rotundo, con múltiples pacientes que se han vuelto independientes de la insulina por más de dos años 3. El VX-880, sin embargo, todavía dependía de la misma inmunosupresión que Lantidra.
Pilar 2: Resolver la Inmunología (El Pivote hacia la Edición Genética)
El siguiente paso era eliminar la necesidad de inmunosupresores. El primer intento, un dispositivo de encapsulación (la primera versión del VX-264), fracasó por baja eficacia. En lugar de insistir, la empresa hizo un pivote estratégico, aprendiendo del error y enfocando todos los recursos en el enfoque más complejo pero definitivo: la edición genética (CRISPR) para crear una célula hipoinmune.
Fuentes de la industria, como Fierce Biotech, reportaron este cambio no como un fracaso, sino como una “demostración de fe en su plataforma de edición genética”, la verdadera joya de la corona de la empresa 4.
3. La Cura Como un Problema de Ingeniería
Hoy, la cura de la DM1 es menos una cuestión de “si” y más una cuestión de “cómo”. Lantidra es la prueba de concepto comercial, pero para un mercado mínimo. Vertex está construyendo la solución industrial. Su ventaja competitiva no reside solo en la célula editada, sino en su capacidad para producirla en masa con calidad (CMC), en su red de hospitales ya entrenada y, como señalan los analistas, en las patentes sobre los métodos de control de calidad que garantizan la seguridad de cada dosis.
Lantidra es un excelente auto conceptual, hecho a mano, para unos pocos. Vertex está construyendo la gigafábrica, la línea de montaje y la red de distribución para el modelo de producción en masa. La aprobación del primero solo hizo que el valor del segundo fuera aún más evidente.
Lecturas Relacionadas
- VX-880: La Fábrica de Células y la Ingeniería de Escala
- VX-264: La Ingeniería de la Célula ‘Invisible’
- El Arma y el Gatillo: Entendiendo los Orígenes de la DT1
Referencias
FDA.gov. “FDA Approves First Cellular Therapy to Treat Patients with Type 1 Diabetes.” Comunicado de Prensa, 28 de Junio de 2023. ↩︎
Krawiec, R. J., et al. “A systematic review of the cost-effectiveness of islet cell transplantation for the treatment of type 1 diabetes.” Diabetes Technology & Therapeutics, 2020. ↩︎
Presentación de datos de Vertex Pharmaceuticals en la 84ª Sesión Científica de la American Diabetes Association (ADA), Junio de 2024. ↩︎
Fierce Biotech. “Vertex axes cell therapy device after early data underwhelm, putting faith in gene-edited prospect.” Noticia, 6 de Febrero de 2024. ↩︎