O que Você Precisa Saber
A possibilidade de usar células-tronco para curar a cegueira inspira manchetes e enche corações de esperança. Para quem convive com a perda de visão devido a doenças degenerativas da retina, é crucial entender o que é fato e o que ainda é promessa.
Este artigo oferece uma visão sóbria e detalhada dos avanços, com foco na terapia celular OpCT-001 da BlueRock Therapeutics.
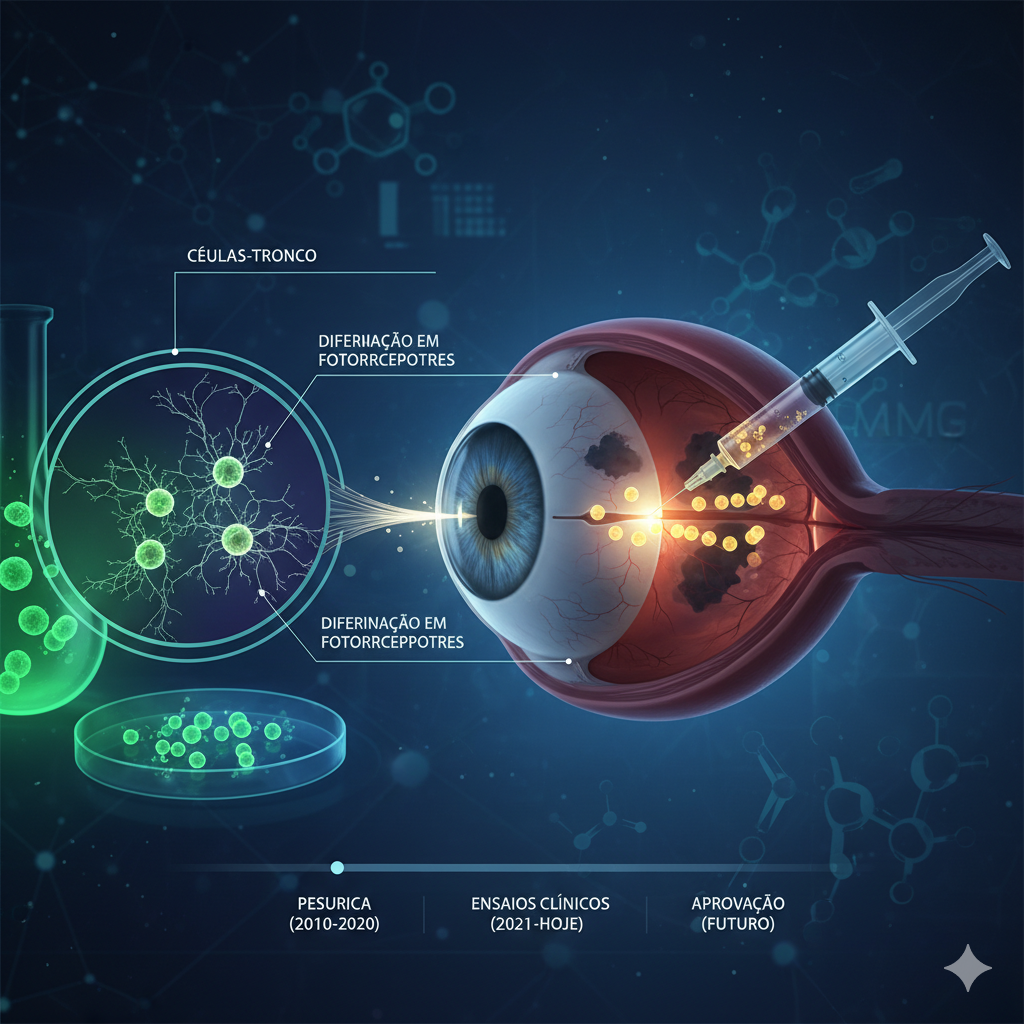
A ideia central é revolucionária: cultivar em laboratório células fotorreceptoras (as células que captam a luz) a partir de células-tronco pluripotentes induzidas (iPSCs). Essas novas células são então injetadas sob a retina do paciente para substituir as que foram destruídas pela doença. O objetivo final é restaurar a capacidade do olho de “enxergar”.
O primeiro ensaio clínico em humanos (Fase 1/2a), registrado sob o identificador NCT05908276, foi autorizado e iniciado 1. O foco principal desta fase inicial não é provar a cura, mas sim avaliar a segurança do procedimento e a tolerabilidade do transplante.
Apesar do enorme potencial, a terapia enfrenta desafios significativos. O principal é a necessidade de medicamentos imunossupressores para evitar que o corpo do paciente rejeite as novas células. Além disso, a tecnologia ainda não foi aprovada para uso comercial e seu custo inicial, quando disponível, será provavelmente muito elevado.

O processo da terapia OpCT-001: do cultivo de células-tronco à sua diferenciação em fotorreceptores e o transplante sub-retiniano. (Crédito da imagem: engeAI.com)
🧬 1. A Ciência: Reconstruindo a Retina
O OpCT-001 visa tratar doenças como a retinite pigmentosa, onde mutações genéticas causam a morte progressiva dos fotorreceptores (cones e bastonetes). Sem eles, a retina perde a capacidade de converter luz em sinais neurais, levando à cegueira.
A terapia da BlueRock atua em três passos principais:
- Criação: Células adultas são reprogramadas em laboratório para se tornarem iPSCs.
- Diferenciação: As iPSCs são cuidadosamente cultivadas para se tornarem células precursoras de fotorreceptores.
- Transplante: A suspensão com milhões dessas novas células é injetada no espaço sub-retiniano para que possam se integrar ao tecido existente 2.
A concessão da designação “Fast Track” pela FDA em fevereiro de 2024 reconhece a seriedade da condição e o potencial da terapia, mas é um facilitador burocrático, não um selo de aprovação 3.
🔬 2. Status do Ensaio Clínico e o que Esperar
O estudo clínico de Fase 1/2a é o primeiro passo em uma longa jornada 1. Seus objetivos são pragmáticos e metódicos.
| Fase do Estudo | Objetivo Primário | O que se Observa |
|---|---|---|
| Fase 1/2a (Atual) | Segurança e Tolerabilidade | Avaliar se o procedimento causa inflamação, rejeição, descolamento de retina ou outros efeitos adversos graves. |
| Fase 2 (Futuro) | Eficácia Preliminar e Dose | Verificar se há sinais de melhora na função visual e determinar a dose ideal de células. |
| Fase 3 (Futuro) | Confirmação da Eficácia | Comparar a terapia com um grupo de controle em um grande número de pacientes para provar o benefício clínico. |
Até o momento, não há dados de eficácia publicados para o OpCT-001 em humanos. Qualquer notícia sobre “cura” é prematura e especulativa.
⚠️ 3. Os Obstáculos Reais no Caminho
A promessa da terapia celular é imensa, mas os desafios são igualmente grandes.
Imunossupressão Contínua: Por usar células de um doador padrão (alogênicas), a terapia exige que o paciente tome medicamentos anti-rejeição. Embora o olho desfrute de certo “privilégio imunológico”, ele não é absoluto 4. Esses fármacos comprometem o sistema imunológico e têm efeitos colaterais próprios.
Integração Celular: Não basta injetar as células; elas precisam sobreviver, se organizar na complexa arquitetura da retina e formar conexões funcionais com os neurónios existentes, um desafio monumental 2.
Realidade da Indústria: O desenvolvimento de uma terapia como essa custa centenas de milhões de dólares. Essa pressão financeira reflete-se nas decisões corporativas. Entre 2023 e 2024, a BlueRock realizou demissões e fechou seu centro de P&D em Cambridge, Massachusetts, para “priorizar o pipeline”, revelando a dura realidade da indústria 5.

O equilíbrio precário entre a pesquisa de longo prazo e as pressões financeiras de curto prazo na indústria de biotecnologia. (Crédito da imagem: engeAI.com)
🔮 4. O Futuro: Esperança Sóbria
O OpCT-001 representa um avanço genuíno. A possibilidade de substituir células perdidas na retina é, pela primeira vez, uma realidade clínica em teste.
No entanto, o caminho para uma cura funcional, segura e acessível é longo. O objetivo final do campo é desenvolver terapias que não exijam imunossupressão, talvez através da edição genética 6. Para pacientes e famílias, a mensagem é de uma esperança cautelosa. A ciência avança, mas o faz em seu próprio ritmo — metódico e rigoroso. A compreensão honesta do processo é o que verdadeiramente nos permite acompanhar e apoiar o avanço da ciência.
Referências
ClinicalTrials.gov. “A Study of OpCT-001 in Adult Participants With Primary Photoreceptor Diseases (STARGAZE).” Identificador NCT05908276. ↩︎ ↩︎
Mandai, M., et al. “Autologous Induced Pluripotent Stem-Cell–Derived Retinal Cells for Macular Degeneration.” New England Journal of Medicine, 2017. ↩︎ ↩︎
BlueRock Therapeutics. Anúncios relacionados à designação “Fast Track” pela FDA, Fevereiro de 2024. ↩︎
Forrester, J.V., et al. “The eye’s immune privilege.” Trends in Immunology, 2008. ↩︎
FierceBiotech. Notícias sobre a reestruturação da BlueRock Therapeutics, 2023-2024. ↩︎
Cyranoski, D. “The CRISPR-edited immune-evading stem cells aiming for universal therapies.” Nature Biotechnology, 2024. ↩︎